Dodekakarbonyl tetrarhodia
| Dodekakarbonyl tetrarhodia | |
|---|---|
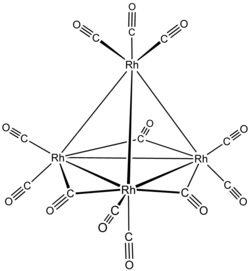 Strukturní vzorec
| |
 Model molekuly
| |
 Vzhled
| |
| Obecné | |
| Systematický název | tri-μ-karbonyl-1:2κ²C;1:3κ²C;2:3κ²C-nonakarbonyl-1κ²C,2κ²C,3κ²C,4κ³C-[Td-(13)-Δ⁴-kloso]-tetrarhodium(6 Rh—Rh) |
| Funkční vzorec | Rh4(CO)12 |
| Sumární vzorec | Rh4C12O12 |
| Identifikace | |
| Registrační číslo CAS | 19584-30-6 |
| EC-no (EINECS/ELINCS/NLP) | 243-171-9 |
| PubChem | 9940312 |
| SMILES | [C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[C-]#[O+].[Rh].[Rh].[Rh].[Rh] |
| InChI | InChI=1S/12CO.4Rh/c12*1-2;;;; |
| Vlastnosti | |
| Molární hmotnost | 747,74 g/mol |
| Bezpečnost | |
| [1] | |
| H-věty | H302 H312 H332[1] |
| P-věty | P261 P264 P270 P271 P280 P301+317 P302+352 P304+340 P317 P321 P330 P362+364[1] |
|
Některá data mohou pocházet z datové položky.
| |
Dodekakarbonyl tetrarhodia je chemická sloučenina se vzorcem Rh4(CO)12. Jedná se o karbonyl rhodia, mající za pokojové teploty podobu tmavě červeného prášku. Používá se v organické syntéze jako katalyzátor.
Příprava, struktura, a reakce
Rh4(CO)12 se připravuje reakcí vodného roztoku chloridu rhoditého s aktivovanou mědí v atmosféře oxidu uhelnatého:[2]
Další možností je reakce methanolového roztoku chloridu rhoditého s CO a následná karbonylace vytvořeného H[RhCl2(CO)2] za přítomnosti citronanu sodného.[3]
Molekula Rh4(CO)12 obsahuje tetraedricky uspořádané čtyři atomy Rh s devíti koncovými a třemi můstkovými CO ligandy; tuto strukturu je možné zapsat jako Rh4(CO)9(μ-CO)3.[3]
Při zahřátí tento komplex může reagovat s fosfiny, L:[4]
- Rh4(CO)12 + n L → Rh4(CO)12-nLn + n CO
Dodekakarbonyl tetrarhodia se ve vroucím hexanu přeměňuje na hexadekakarbonyl hexarhodia:[5]
- 3 Rh4(CO)12 → 2 Rh6(CO)16 + 4 CO
Podobné karbonyly
Karbonyly rhodia jsou, vzhledem ke své podobnosti s katalyzátory hydroformylací, podrobně zkoumány. Vedle nestálého oktakarbonylu dirhodia, Rh2(CO)8, je také znám odpovídající karbonyl kobaltu, Co2(CO)8. Roztoky Rh4(CO)12 se za vysokých tlaků CO mění na Rh2(CO)8:[6]
- Rh4(CO)12 + 4 CO → 2 Rh2(CO)8
Na rozdíl od Co2(CO)8, obsahujícího můstkové karbonyly, jsou v hlavním izomeru Rh2(CO)8 všechny CO ligandy koncové. Nestálost Rh2(CO)8 je analogická náchylnosti Ru(CO)5 k přeměně na Ru3(CO)12.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Tetrarhodium dodecacarbonyl na anglické Wikipedii.
- ↑ a b c https://pubchem.ncbi.nlm.nih.gov/compound/9940312
- ↑ S. Martinengo; G. Giordano; P. Chini. Tri-μ-carbonyl-nonacarbonyltetrarhodium. Inorganic Syntheses. 1990, s. 242–245. doi:10.1002/9780470132593.ch62.
- ↑ a b P. Serp; P. Kalck; R. Feurer; R. Morancho. Tri-μ-carbonyl-nonacarbonyltetrarhodium. Inorganic Syntheses. 1998, s. 284–287. doi:10.1002/9780470132630.ch45.
- ↑ Brian T. Heaton, Luciano Longhetti, D. Michael, P. Mingos, Clive E. Briant, Peter C. Minshall, Brian R. C. Theobald, Luigi Garlaschelli, Ugo Sartorelli. Structural Studies of Rh4(CO)12 Derivatives in Solution and in the Solid State. Journal of Organometallic Chemistry. 1981, s. 333–350. doi:10.1016/S0022-328X(00)93969-X.
- ↑ S. P. Tunik; A. V. Vlasov; V. V. Krivykh. Acetonitrile-Substituted Derivatives of Rh6(CO)16 : Rh 6(CO)16−X(NCMe)X ( X = 1, 2). Inorganic Syntheses. 1977, s. 239–244. ISBN 978-0-471-15288-0. doi:10.1002/9780470132623.ch37.
- ↑ D. T. Brown; T. Eguchi; B. T. Heaton; J. A. Iggo; R. Whyman. High-pressure spectroscopic studies of reactions of the clusters [Rh4(CO)12–x{P(OPh)3}x] (x = 1–4) with carbon monoxide or syngas. Journal of the Chemical Society, Dalton Transactions. 1991, s. 677–683. doi:10.1039/DT9910000677.


