Methyltrioxorhenium
| Methyltrioxorhenium | |
|---|---|
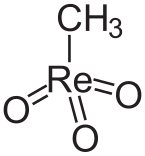 Strukturní vzorec methyltrioxorhenia
| |
 Kuličkový model molekuly methyltrioxorhenia
| |
| Obecné | |
| Systematický název | Methyltrioxorhenium |
| Anglický název | Methylrhenium trioxide |
| Německý název | Methyltrioxorhenium |
| Sumární vzorec | CH3ReO3 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 70197-13-6 |
| PubChem | 2734010 |
| SMILES | C[Re](=O)(=O)=O |
| InChI | InChI=1/CH3.3O.Re/h1H3;;;;/rCH3O3Re/c1-5(2,3)4/h1H3 |
| Vlastnosti | |
| Molární hmotnost | 249,24 g/mol |
| Teplota tání | 112 °C |
| Rozpustnost ve vodě | vysoce rozpustný |
| Bezpečnost | |
|
[1] Varování[1] | |
|
Některá data mohou pocházet z datové položky.
| |
Methyltrioxorhenium (MTO) je organokovová sloučenina se vzorcem CH3ReO3. Je to těkavá, bezbarvá pevná látka používaná jako katalyzátor. Oxidační stav rhenia je +VII, molekula má tvar trigonální pyramidy.[2]
Příprava
Sloučenina je dostupná komerčně, lze ji připravit několika způsoby, typickou metodou je reakce oxidu rhenistého s tetramethylcínem:[3]
- Re2O7 + (CH3)4Sn → CH3ReO3 + (CH3)3SnOReO3
Jsou známy i další alkyl- a arylderiváty. Tyto sloučeniny se chovají jako Lewisovy kyseliny, vytváří adukty 1:1 a 1:2 s halogenidy a aminy.
Využití
Využívá se jako heterogenní katalyzátor v mnoha procesech. Imobilizovaný na Al2O3/SiO2, katalyzuje metatezi olefinů při teplotě 25 °C.[4]
V roztoku katalyzuje oxidace peroxidem vodíku.[5] Terminální alkyny oxiduje na odpovídající kyselinu nebo ester, interní pak na diketony. Oxidace alkenů vede ke tvorbě epoxidů.[5] Také dokáže katalyzovat oxidaci aminů na N-oxidy pomocí peroxouhličitanu sodného.[5][6]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Methylrhenium trioxide na anglické Wikipedii.
- ↑ a b Methyltrioxorhenium(VII). pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ HERRMANN, Wolfgang A.; KIPROF, Paul; RYPDAL, Kristin. Multiple bonds between main-group elements and transition metals. 86. Methyltrioxorhenium(VII) and trioxo(.eta.5-pentamethylcyclopentadienyl)rhenium(VII): structures, spectroscopy and electrochemistry. Journal of the American Chemical Society. 1991-08, roč. 113, čís. 17, s. 6527–6537. Dostupné online [cit. 2021-01-07]. ISSN 0002-7863. DOI 10.1021/ja00017a025. (anglicky)
- ↑ HERRMANN, W.A.; KRATZER, R. M.; FISCHER, R. W. Alkylrhenium Oxides from Perrhenates: A New, Economical Access to Organometallic Oxide Catalysts. Angew. Chem. Int. Ed. Engl.. 1997, roč. 36, čís. 23, s. 2652–2654.
- ↑ KÜHN, Fritz E.; SCHERBAUM, Andrea; HERRMANN, Wolfgang A. Methyltrioxorhenium and its applications in olefin oxidation, metathesis and aldehyde olefination. Journal of Organometallic Chemistry. 2004-11, roč. 689, čís. 24, s. 4149–4164. Dostupné online [cit. 2021-01-07]. DOI 10.1016/j.jorganchem.2004.08.018. (anglicky)
- ↑ a b c MTO - Methyltrioxorhenium. www.organic-chemistry.org [online]. [cit. 2021-01-07]. Dostupné online.
- ↑ JAIN, Suman; JOSEPH, Jomy; SAIN, Bir. Rhenium-Catalyzed Highly Efficient Oxidations of Tertiary Nitrogen Compounds to N -Oxides Using Sodium Percarbonate as Oxygen Source. Synlett. 2006-09, roč. 2006, čís. 16, s. 2661–2663. Dostupné online [cit. 2021-01-06]. ISSN 0936-5214. DOI 10.1055/s-2006-951487. (anglicky) Archivováno 2. 6. 2018 na Wayback Machine.
Externí odkazy
- Obrázky, zvuky či videa k tématu Methyltrioxorhenium na Wikimedia Commons



