Vigabatrin
| Vigabatrin | |
|---|---|
 | |
 | |
| Název (INN) | Sabril |
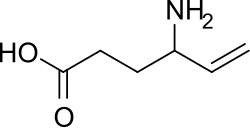
| Název podle IUPAC | (RS)-4-aminohex-5-enoic acid |
| Další názvy | γ-Vinyl-GABA |
| Kódy | |
| Číslo CAS | 60643-86-9 |
| Klasifikace ATC | N03AG04 |
| ChEMBL ID | CHEMBL89598 |
| ChemSpider ID | 5463 |
| PubChem | 5665 |
| Chemie | |
| Sumární vzorec | C6H12NO2 |
| SMILES | C=CC(CCC(=O)O)N |
| InChI | InChI=1S/C6H11NO2/c1-2-5(7)3-4-6(8)9/h2,5H,1,3-4,7H2,(H,8,9) |
| Molární hmotnost | 129.157 g/mol |
| Farmakologie | |
| Kontraindikace | Přecitlivělost na Vigabatrin, mikrokrystalickou celulosu, povidon, sodnou sůl karboxymethylškrobu, magnesium-stearát, hypromelosu, oxid titaničitý nebo makrogol 8000. |
| Cesty podání | orální |
| Biodostupnost | 80-90% |
| Vazba na proteiny | 0% |
| Metabolismus | nemetabolizovaný |
| Vylučování | renální |
| Biologický poločas | 5-8 hodin u dospívajících, u starších lidí 12-13 hodin |
| Další informace | |
| Registrace v ČR | 21/ 566/94-C |
| Dostupnost v ČR | na lékařský předpis |
| Některá data mohou pocházet z datové položky. | |
Vigabatrin, prodávaný pod obchodní značkou Sabril, je lék používaný k léčbě epilepsie. Jako generický lék se objevil v roce 2019. [1]
Účinkuje tak, že zabraňuje rozkladu kyseliny y-aminomáselné (GABA). Vigabatrin, také znám jako y-vinyl-GABA, je strukturním analogem GABA, ale neváže se na receptory GABA.
Lékařské využití
Epilepsie
V Kanadě je vigabatrin schválen pro použití v doplňkové léčbě (s jinými léky) při léčbě rezistentní epilepsie, komplexních parciálních záchvatů, sekundárních generalizovaných záchvatů a pro monoterapii při infantilních křečích u Westova syndromu.
V roce 2003 byl v Mexiku vigabatrin schválen pro léčbu epilepsie, která není dostatečně kontrolována konvenční terapií (pomocná terapie nebo monoterapie), nebo k léčbě na nedávno diagnostikovaných pacientech, kteří nezkoušeli jiné prostředky (monoterapie). [2]
Rovněž bylo naznačeno využití Vigabatrinu k monoterapeutickému použití u sekundárně generalizovaných tonicko-klonických záchvatů, parciálních záchvatů a infantilních křečích v důsledku Westova syndromu.
21. srpna 2009 společnost Lundbeck oznámila, že americká správa potravin a léčiv schválila pro vigabatrin dvě aplikace nového léku. Lék je indikován jako monoterapie u dětských pacientů ve věku jeden měsíc až dva roky s infantilními křečemi, u nichž potenciální přínosy převažují nad potenciálním rizikem ztráty zraku, a jako přídavná (doplňková) terapie u dospělých pacientů s neustupujícími komplexními parciálními záchvaty (CPS), kteří nereagovali adekvátně na několik alternativních léčebných postupů a u nichž potenciální přínosy převažují nad rizikem ztráty zraku.
V roce 1994 Feucht a Brantner-Inthaler uvedli, že vigabatrin snížil záchvaty o 50–100% u 85% dětí s Lennox-Gastautovým syndromem, které měly špatné výsledky s valproátem sodným .
Další
Vigabatrin u zdravých dobrovolníků, kromě zvýšení hladin kortizolu a ACTH, rovněž snížil příznaky panické poruchy vyvolané cholecystokinin tetrapeptidem .
Vigabatrin se také používá k léčbě záchvatů u deficitu sukcinální semialdehyddehydrogenázy (SSADHD), což je vrozený defekt GABA metabolizmu, který způsobuje mentální postižení, hypotonii, záchvaty, poruchy řeči a ataxii hromaděním kyseliny y-hydroxybutyrové (GHB). Vigabatrin pomáhá snižovat hladiny GHB prostřednictvím inhibice GABA transaminázy. To se však děje pouze v mozku, na periferní GABA transaminázu nemá Vigabatrin žádný vliv, takže se GHB v těle stále hromadí a nakonec se dostane až do mozku. [3]
Vedlejší účinky
Centrální nervový systém
Ospalost (12,5%), bolest hlavy (3,8%), závratě (3,8%), nervozita (2,7%), deprese (2,5%), poruchy paměti (2,3%), diplopie (2,2%), agrese (2,0%), ataxie (1,9%), vertigo (1,9%), hyperaktivita (1,8%), ztráta zraku (1,6%) (viz níže), zmatení (1,4%), nespavost (1,3%), narušená koncentrace (1,2%), problémy s osobností (1,1%). Z 299 dětí se 33 (11%) stalo hyperaktivních.
U některých pacientů se během léčby vigabatrinem vyvinula psychóza , která je častější u dospělých než u dětí. K tomu může dojít i u pacientů bez předchozího výskytu psychózy. K dalším vzácným vedlejším účinkům na CNS patří úzkost, emoční labilita, podrážděnost, třes, abnormální chůze a porucha řeči .
Trávicí soustava
Bolesti břicha (1,6%), zácpa (1,4%), zvracení (1,4%) a nevolnost (1,4%). Dyspepsie a zvýšená chuť k jídlu se vyskytla u klinických studií u méně než 1% subjektů.
Celé lidské tělo
Únava (9,2%), přibrání na hmotnosti (5,0%), astenie (1,1%).
Teratogenita
Teratologická studie provedená na králících zjistila, že dávka 150mg/kg/den způsobil rozštěp patra u 2 % mláďat a dávka 200mg/kg/den to způsobila v 9 %. Podle studie zveřejněné v březnu 2001 to může být způsobeno snížením hladin methioninu. V roce 2005 byla zveřejněna studie provedená na University of Catania, která uvádí, že krysy, jejichž matky konzumovaly 250–1000mg/kg/den měly horší výkon ve vodním bludišti a na otevřeném poli, krysy ve skupině 750mg se narodily s podváhou a nedohnaly kontrolní skupinu a krysy ve skupině 1000mg nepřežily těhotenství.
U lidí dosud neexistují žádná kontrolovaná teratologická data.
Smysly
V roce 2003 Frisén a Malmgren prokázali v retrospektivní studii 25 pacientů vigabatrin v nevratně difúzní atrofii vláken nervové sítě sítnice. [4] To má největší vliv na vnější oblast (na rozdíl od makulární nebo centrální oblasti) sítnice. [5] Poruchy zorného pole byly hlášeny již v roce 1997 ve Velké Británii Tomem Ekem a dalšími. Někteří autoři, včetně Comaishe a dalších věří, že ztráta zorného pole a elektrofyziologické změny mohou být prokazatelné až u 50 % uživatelů vigabatrinu.
Retinální toxicitu vigabatrinu lze připsat snížení množství taurinu. [6]
Vzhledem k problémům s bezpečností je FDA vigabatrinovým programem REMS povinen zajistit informovaná rozhodnutí před zahájením a zajistit odpovídající užívání tohoto léku. [7]
Interakce
Studie publikovaná v roce 2002 zjistila, že vigabatrin způsobuje statisticky významné zvýšení plazmatického odbourávání karbamazepinu . [8]
V roce 1984 pánové Dr.Rimmer a Dr.Richens z University of Wales uvedli, že podávání vigabatrinu s fenytoinem snížilo koncentraci fenytoinu v séru u pacientů s epilepsií rezistentní na léčbu. [9] O pět let později stejní dva vědci uvedli pokles koncentrace fenytoinu o 23% během pěti týdnů, a to v článku popisujícím jejich neúspěšný pokus objasnit mechanismus této interakce. [10]
Farmakologie
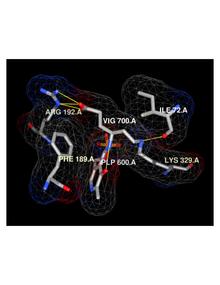
Vigabatrin je nevratný na mechanismu založený inhibitor gama-aminomáselné kyseliny aminotransferázy (GABA-AT), enzymu zodpovědném za katabolismus GABA, který zvyšuje hladinu GABA v mozku. [11] Vigabatrin je racemická sloučenina a jeho [S]-enantiomer je farmakologicky aktivní.
Farmakokinetika
U většiny léčiv je eliminační poločas užitečným předvídačem dávkovacích plánů a doby potřebné k dosažení rovnovážného stavu. V případě vigabatrinu se však zjistilo, že poločas biologické aktivity je mnohem delší než poločas eliminace.
U vigabatrinu neexistuje žádné rozmezí cílových koncentrací, protože vědci nezjistili žádný rozdíl mezi hladinami sérových koncentrací respondentů a hladinami neodpovídajících. Místo toho se předpokládá, že doba působení je více funkcí rychlosti resyntézy GABA-T; hladiny GABA-T se obvykle nevracejí do normálního stavu až do šesti dnů po ukončení léčby.
Historie
Vigabatrin byl vyvinut v 80. letech se zvláštním cílem zvýšit koncentrace GABA v mozku za účelem zastavení epileptického záchvatu. Za tímto účelem bylo léčivo navrženo tak, aby nenávratně zastavovalo GABA transaminázu, která degraduje substrát GABA. Přestože byl tento lék schválen pro léčbu ve Spojeném království v roce 1989, povolené použití vigabatrinu americkým úřadem pro potraviny a léčiva bylo ve Spojených státech do roku 2009 dvakrát odloženo. V roce 1983 to bylo zpožděno, protože pokusy na zvířatech vyvolaly intramyelinický edém, avšak účinky nebyly při pokusech na lidech zřejmé, takže konstrukce léčiv pokračovala. V roce 1997 byly zkoušky dočasně pozastaveny, protože byly spojeny s poruchami periferního zorného pole u lidí.
Společnost a kultura
Obchodní názvy
Vigabatrin se prodává jako Sabril v Kanadě [12] Mexiku, a ve Spojeném království. [13] Obchodní značka v Dánsku je Sabrilex. Sabril byl schválen ve Spojených státech 21. srpna 2009 a v současné době je na trhu v USA prodáván společností Lundbeck Inc., která získala v březnu 2009 amerického sponzora Ovation Pharmaceuticals. V České republice se prodává rovněž pod názvem Sabril.
Generické ekvivalenty
Dne 16. ledna 2019 FDA schválil první generickou verzi Sabrilu (vigabatrinu) ve Spojených státech. [1]
Reference
V tomto článku byl použit překlad textu z článku Vigabatrin na anglické Wikipedii.
- ↑ a b Dostupné online.
- ↑ DEF Mexico: Sabril Archivováno 14. 9. 2005 na Wayback Machine. Diccionario de Especialdades Farmaceuticas. Edicion 49, 2003.
- ↑ Dostupné online.
- ↑ Frisén L, Malmgren K. Characterization of vigabatrin-associated optic atrophy. Acta Ophthalmologica Scandinavica. 2003, s. 466–73. DOI 10.1034/j.1600-0420.2003.00125.x. PMID 14510793. (anglicky)
- ↑ Buncic JR, Westall CA, Panton CM, Munn JR, MacKeen LD, Logan WJ. Characteristic retinal atrophy with secondary "inverse" optic atrophy identifies vigabatrin toxicity in children. Ophthalmology. 2004, s. 1935–42. DOI 10.1016/j.ophtha.2004.03.036. PMID 15465561. (anglicky)
- ↑ GAUCHER D; ARNAULT E; HUSSON Z. Taurine deficiency damages retinal neurones: cone photoreceptors and retinal ganglion cells. Amino Acids. November 2012, s. 1979–1993. DOI 10.1007/s00726-012-1273-3. PMID 22476345. (anglicky)
- ↑ Dostupné online.[nedostupný zdroj]
- ↑ SANCHEZ-ALCARAZ, Agustín; QUINTANA MB; LOPEZ E; RODRIGUEZ I; LLOPIS P. Effect of vigabatrin on the pharmacokinetics of carbamazepine. Journal of Clinical Pharmacology and Therapeutics. 2002, s. 427–30. DOI 10.1046/j.1365-2710.2002.00441.x. PMID 12472982. (anglicky)
- ↑ Rimmer EM, Richens A. Double-blind study of gamma-vinyl GABA in patients with refractory epilepsy. Lancet. 1984, s. 189–90. DOI 10.1016/S0140-6736(84)92112-3. PMID 6141335. (anglicky)
- ↑ Rimmer EM, Richens A. Interaction between vigabatrin and phenytoin. British Journal of Clinical Pharmacology. 1989, s. 27S–33S. DOI 10.1111/j.1365-2125.1989.tb03458.x. PMID 2757906. (anglicky)
- ↑ Long, Phillip W. "Vigabatrin." Archivováno 23. 4. 2006 na Wayback Machine. Internet Mental Health. 1995–2003.
- ↑ drugs.com Vigabatrin Drug Information
- ↑ Treatments for Epilepsy - Vigabatrin Norfolk and Waveney Mental Health Partnership NHS Trust
Externí odkazy
- Obrázky, zvuky či videa k tématu vigabatrin na Wikimedia Commons

