Glutamát-5-semialdehyd
| Glutamát-5-semialdehyd | |
|---|---|
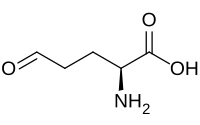 Strukturní vzorec
| |
| Obecné | |
| Systematický název | kyselina (2S)-2-amino-5-oxopentanová |
| Funkční vzorec | OCH(CH2)2CH(NH2)COOH |
| Sumární vzorec | C5H9NO3 |
| Identifikace | |
| Registrační číslo CAS | 2886-91-1 |
| PubChem | 193305 |
| ChEBI | 17232 |
| SMILES | C(C[C@@H](C(=O)O)N)C=O |
| InChI | InChI=1S/C5H9NO3/c6-4(5(8)9)2-1-3-7/h3-4H,1-2,6H2,(H,8,9)/t4-/m0/s1 |
| Vlastnosti | |
| Molární hmotnost | 131,13 g/mol |
|
Některá data mohou pocházet z datové položky.
| |
Glutamát-5-semialdehyd je neproteinogenní aminokyselina účastnící se biosyntézy i rozkladu prolinu a argininu (přes ornitin)[1][2] a biosyntézy antibiotik, například karbapenemů. Vzniká redukcí glutamyl-5-fosfátu glutamát-5-semialdehyddehydrogenázou.
Redukcí této sloučeniny borohydridem sodným vzniká kyselina hydroxyaminovalerová.[3]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Glutamate-5-semialdehyde na anglické Wikipedii.
- ↑ A. Baich. The Biosynthesis of Proline in Escherichia coli: Phosphate-Dependent Glutamate-semialdehyde Dehydrogenase (NADP), the Second Enzyme in the Pathway. Biochimica et Biophysica Acta. 1971, s. 129-134. doi:10.1016/0304-4165(71)90129-2. PMID 4399189.
- ↑ Donald Voet; Judith G. Voet. Biochemistry. [s.l.]: John Wiley & Sons, 2013. Dostupné online. ISBN 978-0-470-57095-1.
- ↑ J. R. Requena; R. L. Levine; E. R. Stadtman. Recent Advances in the Analysis of Oxidized Proteins. Amino Acids. 2003, s. 221-226. doi:10.1007/s00726-003-0012-1. PMID 14661085.

